复星医药创新型肉毒素产品RT002治疗适应症上市申请获受理

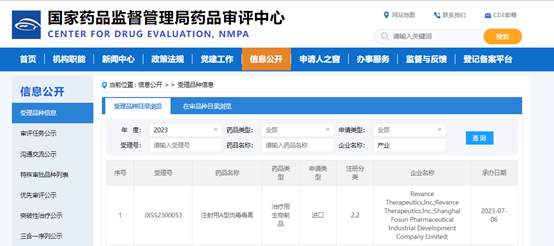
复星医药产业于2018年12月与美国Revance Therapeutics, Inc.(“Revance”)就RT002在中国内地及港澳地区独家使用、进口、销售及其他商业化(不包括制造)等权利许可达成许可协议。
Revance是一家专注于医美创新和治疗产品的生物医药公司,其专业产品和服务组合,包括注射用DAXXIFY®(DaxibotulinumtoxinA型肉毒杆菌毒素)、RHA®系列皮肤填充剂和首个用于医美实践的商业平台OPUL®,可为其合作伙伴及消费者提供定制化的服务。
RT002拟用于美容适应症,如改善成人中度至重度皱眉纹;以及治疗适应症,如成人颈部肌张力障碍。该新药用于改善成人中度至重度皱眉纹的适应症上市申请,已于2022年9月获美国FDA批准,同适应症在中国的上市申请,已于2023年4月获国家药监局受理。截至目前,该新药用于治疗成人颈部肌张力障碍的新适应症上市申请正在接受美国FDA的注册审查。
RT002是一种基于Revance的专有技术平台开发的长效神经调节剂(Neuromodulator),其药物活性成分为Daxibotulinumtoxin A型肉毒杆菌毒素。RT002的制剂中不含辅助蛋白,无人血来源的物质或动物来源的蛋白,稳定肽赋形剂为Revance独有的包含35个氨基酸的专利小肽。RT002无需冷藏即可保持稳定性。III期临床试验结果显示,RT002疗效的中位持续时间为6个月,疗效最长持续时间可达9个月,只需两次治疗就能持续一年的效果。

关于复星医药
上海复星医药(集团)股份有限公司(“复星医药”,股票代码:600196.SH、02196.HK)成立于1994年,是一家植根中国、创新驱动的全球化医药健康产业集团,直接运营的业务包括制药、医疗器械与医学诊断、医疗健康服务。作为国药控股股份有限公司的股东,复星医药将业务范围扩大至药品分销和零售领域。
复星医药以患者为中心、临床需求为导向,通过自主研发、合作开发、许可引进、深度孵化的方式,持续丰富创新产品管线,提升FIC(First-in-class,即同类首创)与BIC(Best-in-class,即同类最佳)新药的研究与临床开发能力,加快创新技术和产品的研发和转化落地。
在“4IN”(创新Innovation、国际化Internationalization、智能化Intelligentization、整合Integration)的战略指导下,复星医药秉承“创新转型、整合运营、稳健增长”的发展模式以及为股东创造价值的信念,不断加强自主研发与外部合作,丰富产品管线,强化全球化布局,提升运营效率,同时,积极推进医疗健康产业线上线下布局,致力于成为全球医疗健康市场的一流企业。
了解公司更多资讯,可登录官网:www.fosunpharma.com。






